1. 서 론
2. 재료 및 방법
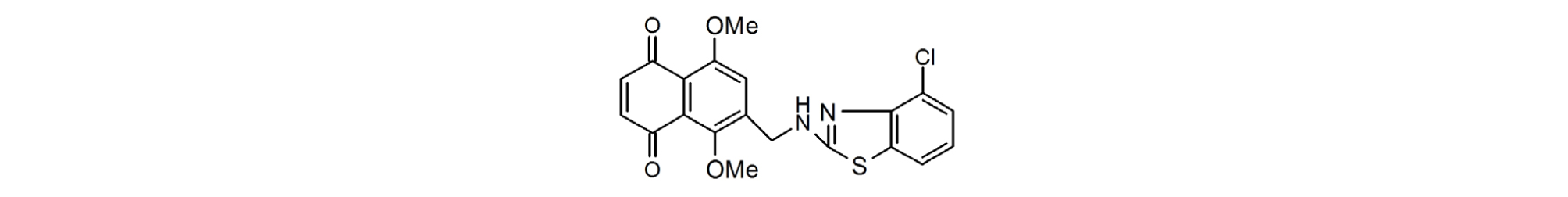
2.1 Naphthoquinone derivatives (NQ 4-6) : 6-((4-chlorobenzothiazol-2-ylamino)methyl-5-8-dimethoxynaphthalene-1,4- dione
2.2 Mesocosm 실험
2.3 Mesocosm (5 ton scale) 내 비생물학적 요인 분석
2.4 Mesocosm (5 ton scale) 내 생물학적 요인 분석
2.5 데이터 분석
3. 결 과
3.1 Mesocosm 내 NQ 4-6 물질의 선택적 제어 효과
3.2 Mesocosm 내 비생물학적 요인에 대한 영향
3.3 생물학적 요인에 대한 영향
4. 고 찰
5. 결 론
1. 서 론
우리나라를 포함한 다양한 많은 국가의 강, 인공호, 댐 및 저수지 등은 이미 대부분 부영양화 되어 유기물 오염이 심각한 상황이다. 유해 조류 대발생 (Harmful algal blooms)은 수계 내 조류 독소 농도 증가와 이・취미 발생으로 수자원으로서의 (수온, 용존 산소, pH, 전기전도도, 영양염)과 생물요인 (박테리아, HNFs, 섬모충, 동물플랑크톤)에 영향을 미치지 않았으며, 대조구와 처리구에서 유사한 경향이 관찰되었다. 즉, NQ 4-6 물질의 현장 적용은 규조 Stephanodiscus sp. 종의 선택적 제어뿐만 아니라, 수생 생물의 서식처와 먹이 공급을 원활하게 함으로써 건강한 수 생태계를 형성하는데 큰 역할을 할 것으로 판단된다. 핵심어: 살조물질, 친환경적 제어, Stephanodiscus 대발생, 나프토퀴논 유도체, 메조코즘 가치 하락과 수중생태계를 교란시킨다 (Bourne et al. 1996, Dawson 1998, Choi et al. 2005). 또한, 정수장 여과지 폐쇄, 응집 침전 등 정수 처리시설에 다량의 응집제가 소요되어 경제적 손실 초래 및 심미적 불쾌함을 유발시켜 관광 및 휴식처로서 가치를 떨어뜨리고 있다 (Lim et al. 2000, Lee et al. 2001, Han et al. 2002). 특히, 저수온기 규조 Stephanodiscus sp. 종은 유럽 (Sommer 1986, Leitao 1995), 아프리카 (Kilham et al. 1986), 아시아 (Kang et al. 2005, Jung et al. 2009, Kang et al. 2012) 등 전세계적으로 발생하고 있다. 우리나라의 경우, 낙동강 및 한강에서 저온 갈수기에 장기간 발생하며, 강과 호소에서 번무하여 수질을 악화시키는 주 원인으로 보고되고 있다 (Han et al. 2002, Ha et al. 2003). 특히 매년 낙동강에서 우점하여 현장 식물플랑크톤의 95% 이상에 해당하는 밀도를 차지해 마치 단일 배양한 것처럼 갈색의 물띠를 형성하는 것으로 알려져 있다 (Cho et al. 1998, Jung et al. 2008).
유해 조류를 제어하는 방법으로 조류 제거선을 이용한 기계적 수거, 초음파, 산소발생 등의 물리적 방법, 살조제, 응집제, 산화제 등의 물질을 이용한 화학적 제어 방법, 미생물이 분비하는 물질에 의한 분해, 동물플랑크톤 등의 천적생물을 인위적으로 투여하여 제거하는 생물학적 방법이 있다 (Sigee et al. 1999, Gumbo et al. 2008, Foflonker 2009). 현재까지 다양한 방면에서 다양한 기술이 개발되었으나, 현장에서의 제어 효율, 경제성, 독성 발생 등의 문제점에 의해 현장에서 사용 가능한 기술은 드문 실정이다. 따라서, 본 연구진은 제시된 많은 한계점을 극복하고 실제 녹조 대발생 현장에 적용하기 위한 기법으로 다양한 식물 추출물과 미생물에서 생산되며, 항암제 (antitumor), 항증식제 (antiproliferative), 항혈소판제 (antiplatelet), 항염증제 (anti-inflammatory), 항알레르기제 (antiallergic), 말라리아 치료제 (antimalarial) 등의 기능 (O’Brien 1991, Monks et al. 1992, Dong et al. 2009, Menna-Baretto et al. 2009)뿐만 아니라, 다양한 세균, 곰팡이, 바이러스 등에도 효과적인 제어 효과를 보이는 생물 유래물질 Naphthoquinone (NQ) 물질을 기반으로 친환경적인 새로운 녹조 제어 물질을 개발하였다 (Byeon 2013, Byun et al. 2015, Joo et al. 2016a, Joo et al. 2017). 그러나, 최종 선정된 물질은 현장 조건에서의 살조효과와 다른 생물학적 요인과 비생물학적 요인에 대한 평가는 이루어 지지 않았다. 따라서, 본 연구에서는 규조 Stephanodiscus sp. 제어를 위해 개발된 물질의 현장 적용 가능성을 평가하기 위해 mesocosm 실험을 통해 확인하고자 하였다. Mesocosm 실험은 실제 현장에서 자연 생태계 시스템의 기능과 구조를 단순화 시킨 생태계 실험의 방법으로 수 생태계 연구에 유용한 방법으로 사용되고 있다. 특히, 화학적인 교란 혹은 새로운 환경조건 (수온 상승, CO2 농도 증가, 새로운 화학물질 등)이 수 생태계에 작용되었을 때 생태계 반응을 평가하기 좋은 방법이다 (Ahn et al. 2001, Naito et al. 2003, Orihel et al. 2006). 더구나, 유해 조류가 발생한 현장수를 이용한 mesocosm 실험은 실험실에서 확인된 살조물질의 효과를 현장 유사 생태계 내에서 검증하고, 적용 시 발생할 수 있는 살조효과 및 독성에 의한 생태계 교란에 대한 요인들을 현장 적용 이전에 확인할 수 있기 때문에 (Odum and Odum 2003, Willis et al. 2004) 실험실 내 연구결과와 실제 현장 적용 사이의 차이를 줄일 수 있는 중요한 실험이다 (Han et al. 1995, Wirth et al. 2004).
본 연구에서는 실험실 내에서 S. hantzschii에 대하여 조류 제어 효과가 입증된 NQ 물질이 실험 규모가 커짐에 따른 제어 효과 감소 문제와 수생태계 미치는 영향을 평가하고자 실제 현장에 존재하는 Stephanodiscus sp. 종에 대하여 mesocosm 실험을 수행하여 NQ 물질의 실용가능성을 확인하고자 하였다.
2. 재료 및 방법
2.1 Naphthoquinone derivatives (NQ 4-6) : 6-((4-chlorobenzothiazol-2-ylamino)methyl-5-8-dimethoxynaphthalene-1,4- dione
4-chloro-N-((1,4,5,8-tetramethoxynaphthalene-2-yl)methyl)benzo thiazol-2-amine 861.1 mg (1.95 mmol)과 acetone 20 mL을 넣고 실온에서 H2SO4 164 µL (2.93 mmol), H2O 4 mL, CrO3 203.2 mg (1.95 mmol) 넣는다. 이 혼합물을 실온에서 1시간 교반시킨 뒤 methylene chloride와 물로 추출 한 후에 methylene chloride 층을 모아 무수 황산마그네슘으로 수분을 제거한 다음 감압건조 하였다. 화합물을 컬럼 크로마토그래피 (hexanes: EtOAc=2:1)로 정제하여 목적 화합물을 얻었다. 최종 합성된 NQ 4-6 물질의 기본 구조는 Fig. 1과 같으며, 본 실험에 사용한 naphthoquinone 유도체는 조선대학교 조훈 교수팀 연구실에서 합성하여 제공받았다.
2.2 Mesocosm 실험
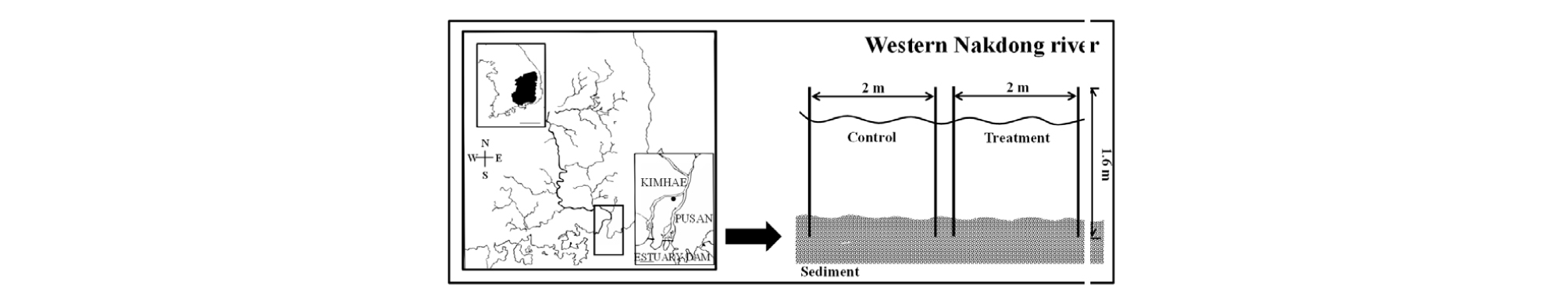
Stephanodiscus sp.에 의한 녹조 발생은 최근 매년 중위도 지역의 호수, 하천, 연못 등 담수에서 발생하지만 특히 낙동강 (35-37°N, 124-131°E)에서 큰 문제를 발생시켜왔다. 5 ton 규모 mesocosm 실험은 현장의 식물플랑크톤 군집 (assemblage)과 다른 요인 변화 조사를 목적으로 수행되었으며, 수심과 저질의 경사 조사 후 서낙동강 (35°13’34”N, 128°59’09”E) 내 설치하여 수행하였다. Mesocosm 실험 수행을 위해 FRP (Fiber Reinforced Plastics) 재질의 윗면과 아랫면이 뚫린 형태의 개구형 원통 (cylindrical) tank (직경 2 m, 높이 1.8 m)를 대조구와 NQ 4-6 물질 실험구 각 2개씩 서낙동강 지역에 설치하였다 (Fig. 2). 실제 현장 조건의 실험을 수행하기 위해 tank의 바닥을 현장 sediment에 고정시켜 바닥과 표면이 노출된 형태로 수행하였다. NQ 4-6 물질을 3 L의 현장수로 잘 풀어준 후, Stephanodiscus sp. 종이 4 × 103 cells mL-1 밀도로 번성한 현장수에 선행 연구에서 최적의 살조효과를 나타낸 0.2 µM 농도로 NQ 4-6 물질을 접종하였다. 분석을 위한 샘플링은 매일 AM 11:00에 2 L beaker로 표층수를 채수하였다.
2.3 Mesocosm (5 ton scale) 내 비생물학적 요인 분석
수온, pH, 전기전도도, 탁도, 용존산소는 portable multi-parameter (HORIBA U50, Japan)으로 0일차부터 10일차까지 매일 측정하였다. 또한, 샘플링에 앞서 각각의 실험구에 PVC pipe를 이용하여 수층을 잘 혼합시켜 저층 바닥에 가라앉은 (bottom-dwelling) 미생물들을 부유시켜 주었다. 샘플은 접종 당일부터 10일차까지 매일 각 실험구의 표층수에서 1 L의 polyethylene bottle로 채수하였다. 염양염 (Phosphate: PO4-P, Silicate: SiO2-Si) 분석을 위해 채수 일자에 250 mL을 실험구와 대조구에서 각각 채수하여 glass fiber filter (GF/F) (Whatman International, Maidstone, UK)로 여과한 후 산처리된 polyethylene bottle에 50 mL씩 나누어 −70°C deep freezer에 보존하였다. 모든 영양염 분석은 APHA (2005)에 의거하여 각각 분석하였다.
2.4 Mesocosm (5 ton scale) 내 생물학적 요인 분석
박테리아 (bacteria), 종속영양 미소편모류 (heterotrophic nanoflagellates: HNFs), 식물플랑크톤 (phytoplankton)의 세포를 계수하기 위해 샘플 1 L 채수 후, 산처리된 300 mL의 polyethylene bottle에 담아 glutaraldehyde (final concentration 2%)로 고정하여 4°C에서 암소 보관하였다.
박테리아와 HNFs의 경우, 각각 2 mL, 10 mL을 분취하고 아래와 같은 방법으로 직접 계수해주었다 (Riemann et al. 1990). 각각의 샘플은 DAPI (5 µg mL-1 final concentration)로 5분간 염색한 후, black 0.2 µm pore size polycarbonate filters (poretics)하에서 포집하고, 1,000 배율 (magnification)의 Zeiss Axioplan epifluorescence microscope 하에서 백색으로 발광하는 세포를 계수하였다. 대략, > 200 cells filter-1 (또는 > 10 fields filter-1)의 세포수를 계수하였다. HNFs의 경우, flagellate 크기를 가진 세포이며 red chlorophyll fluorescence (visible chlorophyll)가 관찰되면 HNFs로 간주하였다 (Round et al. 1990). HNFs와 protozooplankton (예: ciliates, amoebae)의 구별은 Patterson (2003)의 방법대로 접안렌즈 내의 calibrated ocular grid를 사용해 크기 별로 group화하여 분별해 주었다. 이 방법으로는 HNFs의 정확한 수를 계수할 수는 없지만, 샘플들 사이의 세포수 변화 경향을 확인할 수 있는 좋은 방법이다. 개별 flagellate의 크기는 calibrated ocular grid를 사용해 측정하였다.
식물플랑크톤의 계수를 위해 1 mL을 분취해 Sedgwick- Rafter counting chamber (Phyco-Tech Inc., USA)를 사용하여 200 magnification로 IX71 inverted microscope (Olympus, Japan) 하에서 계수하였다. 대상 조류인 Stephanodiscus sp.의 개체수와 식물플랑크톤 총 생물량 관찰을 위한 Chlorophyll-a 변화를 측정하였으며, 접종 전일부터 10일까지 변화를 관찰하였다. 식물플랑크톤의 동정은 광학 현미경 (Olympus IX71, Japan)의 200-400 magnification에서 Sedgwick-Rafter Chamber (PhytoTech Inc., USA)를 이용하여 종 수준까지 동정하였고, 동일 속에서 뚜렷한 식별 형질의 차이를 보이지 않는 종은 미동정종 (sp.)으로 처리하였다.
2.5 데이터 분석
NQ 4-6 물질에 의한 살조효과 또는 살조활성 (algicidal activity)은 다음 식으로 계산하였다.
Algicidal activity (%) = (1-Tt/Ct) × 100
이때 T (처리구)와 C (대조구)는 각각 물질이 접종되었을 때와 접종되지 않았을 때의 조류 세포수이며, t는 처리 기간 (day)수를 의미한다.
3. 결 과
3.1 Mesocosm 내 NQ 4-6 물질의 선택적 제어 효과
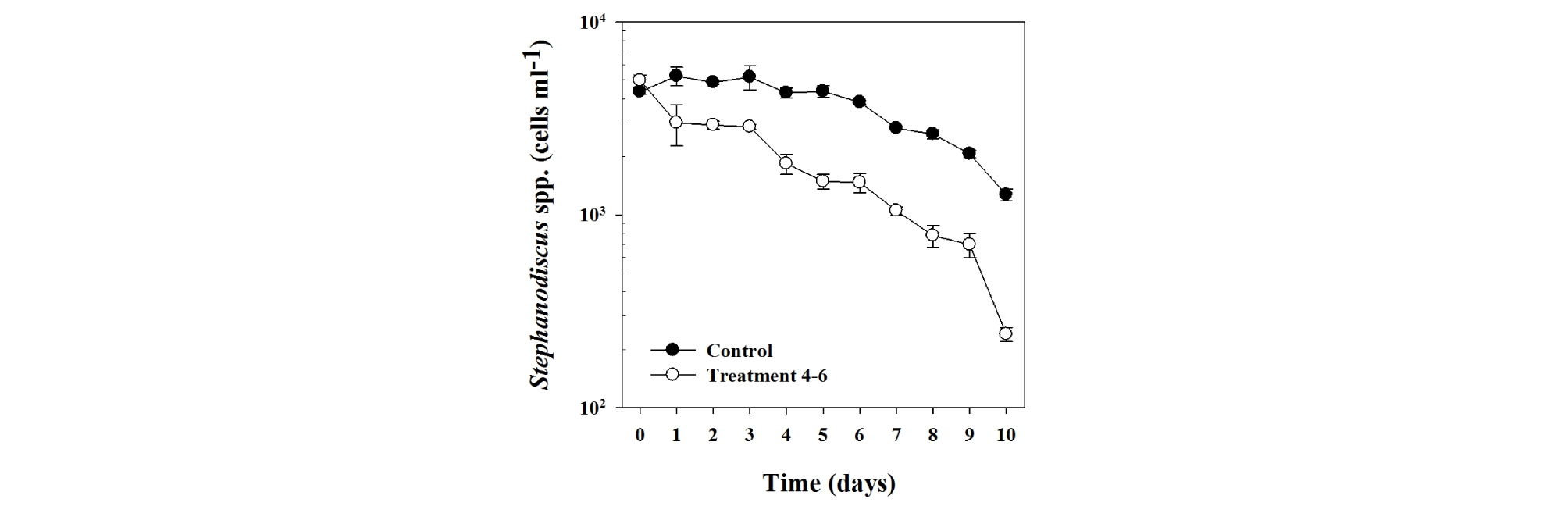
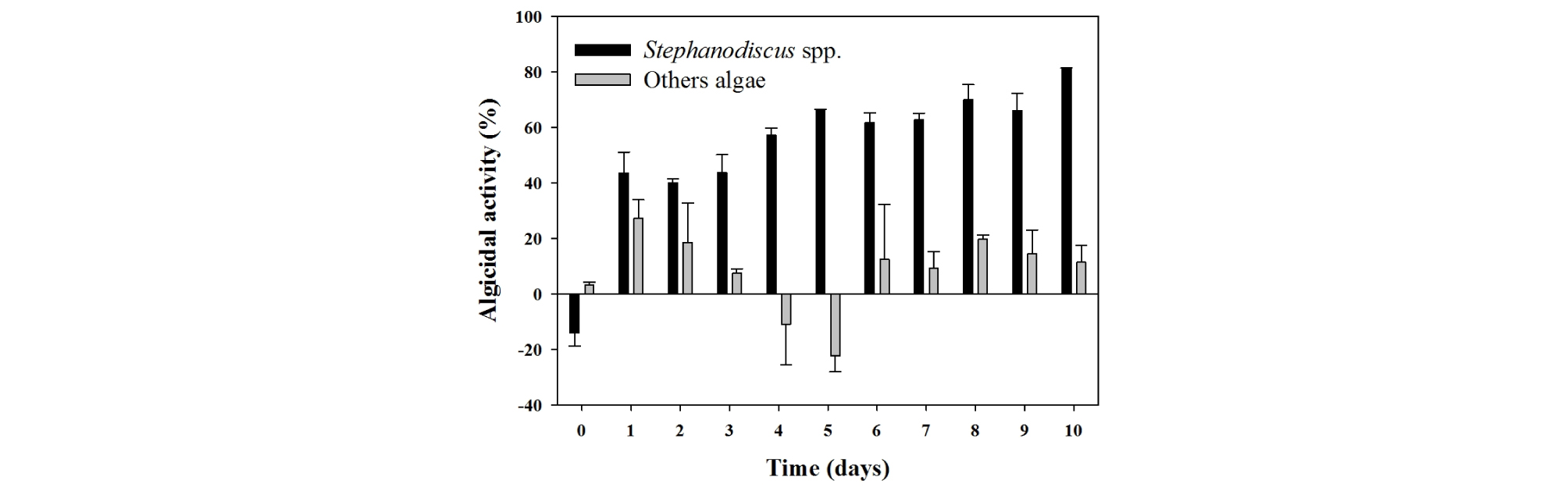
서낙동강 현장에서 5 ton 규모로 진행된 mesocosm 실험은 실험실 내에서의 결과와 유사하게 관찰되었다. NQ 4-6 물질을 접종하지 않은 대조구 내 Stephanodiscus sp. 세포수는 실험 초기 (4.4 ± 0.1) × 103 cells mL-1에서 실험 경과 7일차 (4.3 ± 0.05) × 103 cells mL-1 정도의 세포밀도로 유지하다가 점차 감소하여 실험 종료시인 10일차에는 (1.3 ± 0.09) × 103 cells mL-1로 감소하였다 (Fig. 3). 그러나, NQ 4-6 물질을 접종한 처리구에서는 대상 조류인 Stephanodiscus sp. 종이 실험 초기 (5.0 ± 0.3) × 103 cells mL1에서 접종 후 1일차에는 (3.0 ± 0.7) × 103 cells mL-1로 감소하였으며, 이 후 급격하게 감소하여 실험 종료시인 10일차에는 (0.2 ± 0.02) × 103 cells mL-1으로 세포가 대부분 사멸되었다. 이를 바탕으로 대상 조류인 Stephanodiscus sp.에 대한 살조효과를 분석한 결과, 접종 당일은 Stephanodiscus sp. 종에 대하여 대조구 대비 살조효과는 관찰되지 않았으나 접종 1일 경과 후 36%의 살조효과가 관찰되었다 (Fig. 4). 이 후, 점진적으로 살조효과가 증가하여 실험 종료시인 10일차에는 81%의 살조효과가 관찰되었다. 반면, mesocosm 내 다른 조류에 대한 영향은 거의 관찰되지 않았다.
3.2 Mesocosm 내 비생물학적 요인에 대한 영향
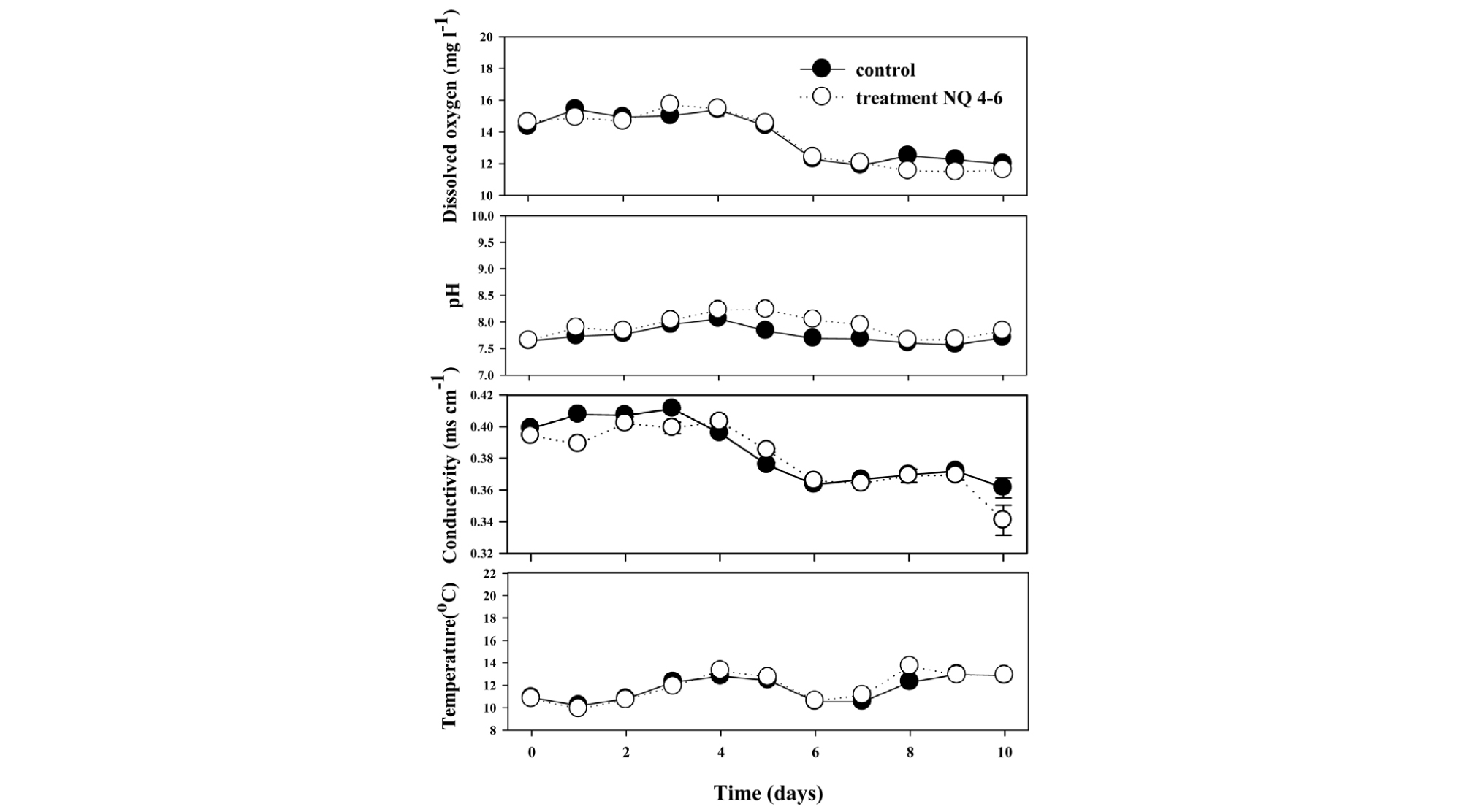
낙동강 현장에서 규조 Stephanodiscus sp.를 대상으로 한 NQ 4-6 물질의 5 ton 규모의 mesocosm 실험에서 다양한 물리・화학적 요인 (physicochemical factors)의 시간에 따른 변화를 관찰하였다. Mesocosm 내 수온의 경우, 대조구와 NQ 4-6 물질을 접종한 처리구 모두에서 실험기간 동안 비교적 낮게 유지되었으나, 시간이 흐름에 따라 10.2°C에서 13.7°C까지 증가하였으며, 대조구와 NQ 4-6 물질을 처리한 실험구에서 모두 유사하게 관찰되었다 (Fig. 5). 전기전도도는 실험기간 동안 대조구와 NQ 4-6 물질을 처리한 실험구에서 유사하게 관찰되었으며, NQ 4-6 물질을 접종한 당일 0.398 ± 0.003 ms cm-1에서 실험 종료 시인 10일차에는 0.340 ± 0.015 ms cm-1로 소폭 감소하였다. 용존산소 역시 대조구와 처리구에서 유사한 농도가 관찰되었으며, 실험 초기 14.3 ± 0.1 mg L-1에서 종료시인 10일차에는 11.6 ± 0.06 mg L-1로 감소하는 경향이 관찰되었다. pH의 경우, 실험기간 동안 대조구와 처리구 모두 7.5에서 8.2 사이로 계속 유지되었으며, 대조구와 처리구별 큰 차이가 관찰되지 않았다 (Fig. 5).
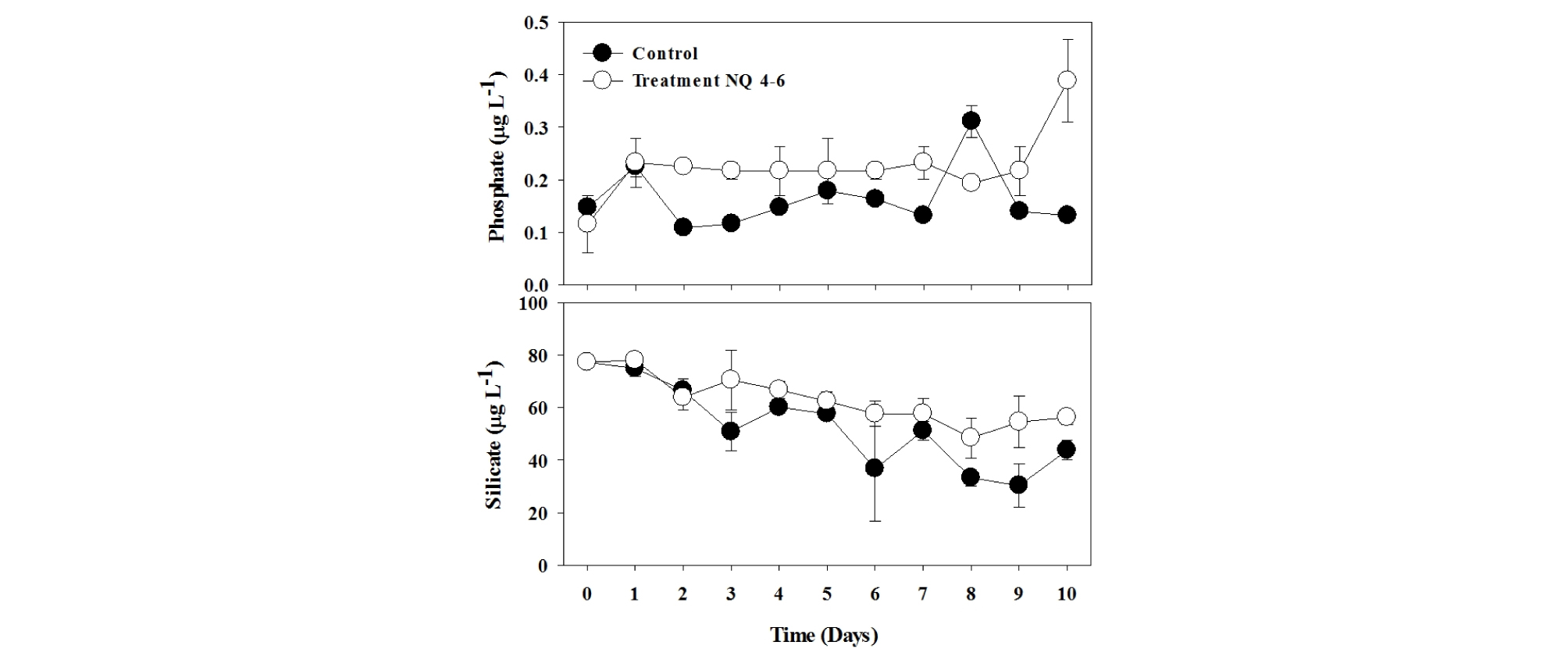
NQ 4-6 물질의 제어 대상 조류인 규조 Stephanodiscus sp. 종의 성장에 가장 큰 영향을 줄 수 있는 영양염인 인산염인 (Phosphate: PO4-P)과 규산규소 (Silicate: SiO2-Si) 농도 변화를 관찰하였다 (Fig. 6). 그 결과, 인산염인의 경우, 접종 당일부터 10일차까지 대조구는 0.1 µg L-1 농도로 거의 유지되었으며, NQ 4-6 물질을 처리한 실험구에서는 1일차 이후 0.2 µg L-1 농도로 관찰되어 대조구보다 다소 높게 유지되었다. 규산규소의 경우는 2일차까지 대조구와 처리구에서 유사한 경향이었으나, 3일차부터는 대조구에서 농도가 감소하기 시작하여 대조구는 50 µg L-1, 처리구는 70 µg L-1의 농도로 관찰되었다. 이 후, 실험 기간 동안 대조구에 비해 NQ 4-6 물질을 처리한 실험구에서 다소 높은 농도로 유지되었다 (Fig. 4).
3.3 생물학적 요인에 대한 영향
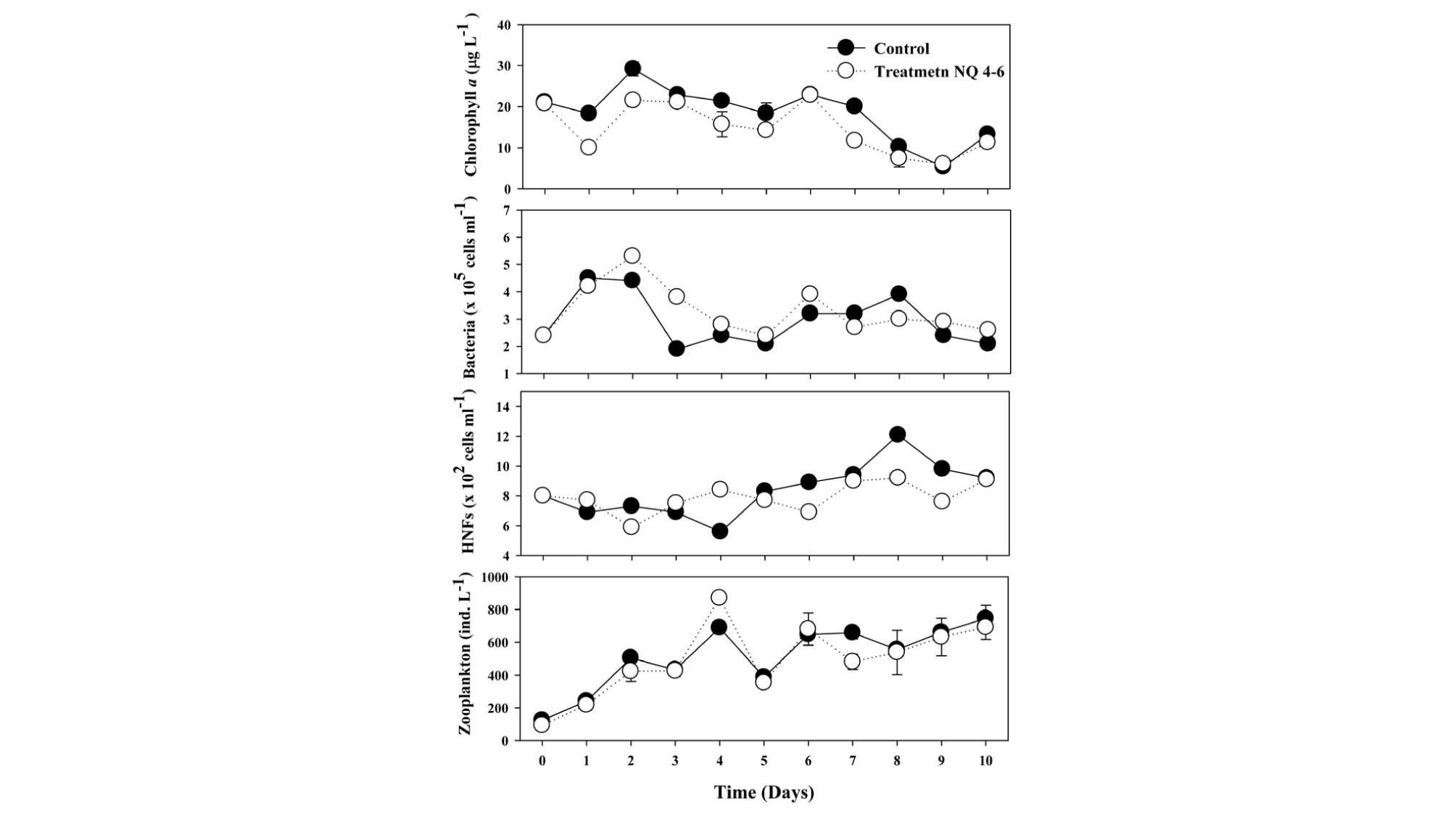
Mesocosm 내 전체 식물플랑크톤의 생물량 변화 관찰을 위해 Chlorophyll-a 농도를 분석한 결과, 대조구에서는 접종 당일 21.06 ± 0 µg L-1에서 2일 경과 후 29.15 ± 1.21 µg L-1까지 증가하였으나, 이 후 점차 감소하는 경향을 보였다 (Fig. 7). 이 후, 실험 종료시인 10일차에는 13.25 ± 0.67 µg L-1까지 감소하였다. 그러나, NQ 4-6 물질을 접종한 처리구에서는 접종 당일 20.72 ± 0 µg L-1에서 1일차 9.99 ± 0.01 µg L-1로 급격하게 감소 후, 소폭 증가하여 실험 종료시인 10일차에는 11.33 ± 0.34 µg L-1의 농도가 관찰되었다.
박테리아의 경우, 대조구와 NQ 4-6 물질을 처리한 실험구 모두에서 실험기간 동안 유사한 경향이 관찰되었다. NQ 4-6 물질 접종 당일 (2.4 ± 0.2) × 105 cells mL-1의 세포밀도에서 실험 종료시인 10일차에는 대조구 (2.1 ± 0.4) × 105 cells mL-1, 처리구 (2.6 ± 0.08) × 105 cells mL-1로 큰 변화 없이 모든 실험구에서 일정하게 유지되는 것을 확인할 수 있었다 (Fig. 7). HNFs 역시 박테리아 변화와 유사하게 실험기간 동안 대조구와 처리구 모두 유사한 경향으로 관찰되었다 (Fig. 7). NQ 4-6 물질을 접종한 당일 대조구와 처리구 모두 (8 ± 0.1) × 102 cells mL-1에서 실험 종료시인 10일차에는 대조구는 (9.1 ± 1.2) × 102 cells mL-1, 처리구는 (9.2 ± 0.7) × 102 cells mL-1의 세포밀도가 관찰되었다. 동물플랑크톤의 경우, 실험기간 동안 대조구와 NQ 4-6 물질을 처리한 실험구 모두 점진적으로 증가하였다 (Fig. 7). NQ 4-6 물질의 접종 당일 동물플랑크톤 세포수는 대조구 123.9 ± 3.3 individual L-1, 처리구 93.3 ± 14.6 individual L-1에서 실험 종료시인 10일차에는 대조구 746.2 ± 78.7 individual L-1, 처리구 691.8 ± 74.3 individual L-1로 대조구와 처리구에서 모두 증가하는 유사한 경향이 관찰되었다.
4. 고 찰
녹조 현상을 제어하는 방법으로 기계적 수거, 초음파, 전기분해 등의 물리적 제어방법, 응집 및 침전제, 산화제 등의 화학적 제어방법, 생물에 의한 유기물 산화에 의한 분해, 섭식하여 제거하는 미생물과 어패류를 인위적으로 투여하여 제거하는 생물학적 제어방법이 있다 (Sigee et al. 1999, Gumbo et al. 2008, Foflonker 2009). 그러나, 대부분의 기술이 유해 남조류 제어를 위한 기술로 현재까지 규조 Stephanodiscus sp. 제어를 위한 연구는 Pseudomonas fluorescens (Kang et al. 2007, Jung et al. 2009), Pseudomonas putida (Kim et al. 2004), Stentor roeseli (Kim et al. 2004) 등 대부분 박테리아, 섬모충과 같은 생물학적 제어 방법만 연구되어 왔다. 이러한 생물학적 방법은 수중 생태계의 급격한 혼란을 막고 현장에서 서식하는 소비자를 이용한다는 점에서 이상적인 방법으로 논의되고 있으나, 현재까지 현장에 직접 이용한 사례는 극히 드문 실정이다. 또한, 조류 제어를 위한 특정 생물군의 적용은 실제 수중 내에서 대상 조류와 생물제재간의 단순한 1:1 관계만을 고려하기 어려우며, 생물간의 상호 관계를 고려하지 않고 적용한다는 건 매우 부정적인 결과를 얻기 쉽다 (Kim and Han. 2003). 실제로 기 개발된 다양한 녹조 제어 기술 대부분은 실험실에서의 소규모 실험에서는 대상 조류에 대해 높은 제어 효과를 입증하였으나, 처리 용량이 커지거나 실제 수계에서는 다양한 요인에 의해 제어 효과가 미미한 경우가 빈번히 발생하였다 (Schrader et al. 2003). 개발된 살조물질의 현장 적용에 앞서, 현장에 존재하는 대상 조류의 제어 효과 확인과 다양한 요인의 모니터링을 통한 현장 적용 가능성을 평가하는 것이 반드시 필요하다. 따라서, 본 연구에서는 최종 선정된 물질을 현장에 설치한 mesocosm 실험을 통해 현장에서의 효과 및 생태계 변화를 확인하고자 하였다. 더구나, natural sediment가 존재하는 조건으로 수행한 mesocosm 실험은 단순히 현장의 대상 조류 제어 효과 확인뿐만 아니라, 실제 현장에서 사용 시 sediment 내 다양한 요인들에 의해 변화될 수 있는 제어 효과를 확인 할 수 있는 실험이다. 즉, 물질이 상용화되었을 때의 문제점을 확인할 수 있는 조건으로 실험실 내의 소규모 실험이 아닌 큰 규모 실험에서의 살조효과 분석 및 신규 물질의 생태계 적용 시 발생 가능한 문제점의 확인을 위한 목적으로 수행되었다.
본 연구에서 사용된 생물유래 물질 naphthoquinone은 여러 가지 기능에 의해 의약품 (medical supplies), 제초제 (herbicide), 살균제 (antimicrobial agent) 등 다양한 용도로 사용되고 있다 (Schrader et al. 2003). 뿐만 아니라, 자연상태에서 산화-환원 반응을 조절하는 물질로 쓰이며 (Harn et al. 2010), 비타민 K와 유사한 화학적 구조를 갖고 있다고 보고되었다 (Combs et al. 1976). 이러한 특성을 바탕으로 현장에서 친환경적 녹조 제어가 가능할 것으로 판단되어 naphthoquinone을 후보물질로 선택하였다. 본 연구진는 선행연구를 통해 기존의 naphthoquinone 유도체 (1,4-naphthoquinone과 9,10-anthraquinone 등)과는 다르게 골격구조 변화로 신규 유도체를 합성하였고, 실험실 내 microplate, microcosm 실험을 통해 담수 규조 Stephanodiscus sp.에 대한 살조효과를 입증하였다 (Byun et al. 2015, Joo et al. 2016a). 또한, Joo et al. (2016a)의 NQ 4-6 물질 생태독성 연구를 통해 미세조류 Selenastrum capricornutum는 2.8 µM, 동물플랑크톤 Daphnia magna는 14.0 µM, 어류 Danio rerio는 14.6 µM의 LC50 값을 확인하였으며, 이는 mesocosm 실험에 접종한 0.2 µM의 농도보다 높은 농도로서 다른 생물에 대한 독성이 없을 것으로 판단하였다. 그러나, 최종 선정된 NQ 4-6 물질의 현장에서 살조효과와 먹이사슬을 고려한 수생태계 내 미치는 전반적인 영향 평가가 이루어지지 않아 실제 Stephanodiscus sp.가 우점한 서낙동강에 수계 내 물을 가두는 형태의 실험구를 설치하여 살조효과 및 비・생물학적 요인에 대하여 연구하고자 하였다.
서낙동강 현장에서 수행한 mesocosm 실험은 실험실 내 결과를 바탕으로 NQ 4-6 물질을 최종농도 0.2 µM로 접종하였으며, 접종 10일 경과 후 81%의 높은 살조효과가 관찰되었다 (Fig. 4). 처리 용량의 증가 및 살조효과를 변화시킬 수 있는 요인이 존재하는 현장에서의 실험임에도 불구하고 실험실 내 microplate, microcosm 실험 결과와 유사하게 NQ 4-6 물질 접종 1일 후부터 대상 조류 Stephanodiscus sp.의 급격한 감소가 관찰되었다. 다만, 대조구 내 Stephanodiscus sp. 개체수가 6일 이 후 다소 감소하는 경향이 관찰되었으나, 이러한 결과는 아랫면이 저질층에 노출된 형태의 mesocosm 실험구가 외부 물을 완벽하게 차단하지 못하면서 발생하는 영양염 감소 등의 다양한 요인에 노출되어 감소한 것으로 판단된다. 뿐만 아니라, Joo et al. (2016a)의 현장수를 이용한 microcosm 연구 결과와 동일하게 접종 당일부터 대상 조류 Stephanodiscus sp. 종만을 선택적으로 제어하는 결과가 관찰되었다. 살조효과가 변할 수 있는 다양한 요인이 있는 현장임에도 불구하고 실험실 내 결과와 유사한 결과가 관찰된 것은 현장에서의 성공 가능성이 매우 높다는 것을 의미하며, NQ 4-6 물질의 Stephanodiscus sp. 제어 효과에 대한 재현성이 추가 입증되었다고 판단된다. 더구나, NQ 4-6 물질은 µM 수준의 저 농도만으로도 대상 조류를 선택적으로 제어하여 다른 수생생물에 대한 영향을 최소화할 수 있으며, 경제적으로 적용할 수 있는 기술이라 판단된다.
다양한 요인이 존재하는 현장의 mesocosm 실험임에도 불구하고 NQ 4-6 물질을 접종한 처리구에서 수온, 용존산소, 전기전도도, pH와 같은 환경요인이 대조구와 유사한 경향으로 변화됨을 확인하였다 (Fig. 5). 다만, 인산염인 (PO4-P), 규산규소 (SiO2-Si)의 영양염에서 NQ 4-6 물질을 접종한 처리구에서는 대조구에 비해 높게 유지되는 것을 관찰하였다 (Fig. 6). 이러한 결과는 기존의 연구결과와 유사한 결과로서, 높은 밀도로 존재하던 규조 Stephanodiscus sp. 종이 NQ 4-6 물질에 의해 사멸됨에 따라 영양염이 용출된 것으로 판단된다. 이로 인해, Stephanodiscus sp. 세포로부터 용출되는 영양염에 의해 일시적으로 높은 농도가 측정된 것으로 판단되나, 현장에서의 변화 가능한 범위 내에서의 유동적인 변화로서 생태계 미치는 영향은 없을 것이라 판단된다.
또한, 박테리아, HNFs는 실험기간 동안 대조구와 NQ 4-6 물질을 접종한 실험구에서 유사한 변동량을 나타내었다 (Fig. 7). 뿐만 아니라, 동물플랑크톤은 실험 종료일까지 대조구와 처리구에서 점진적으로 증가하는 경향을 보였다. 이러한 생물학적 요인의 변동량을 비추어 볼 때, EPA, OECD에서 지정한 지표생물이 아닌 현장에 존재하는 다양한 생물을 이용하여 직접적으로 생태계 미치는 독성을 평가하였다고 생각되며, 제어하고자 하는 Stephanodiscus sp. 세포 이외의 다른 생물들에게는 영향을 미치지 않음을 확인하였다. 따라서, 본 mesocosm 실험을 통해 현장에서의 살조효과 감소, 종천이와 새로운 조류에 의한 녹조 발생 문제와 생태독성 및 생태계 교란 문제가 없음이 재확인되었으며, 규조 Stephanodiscus sp. 제어를 위해 NQ 4-6 물질이 친환경적으로 사용될 것이라 판단된다.
5. 결 론
겨울철 규조 Stephanodiscus sp. 종의 발생에 의한 경제적 피해를 막고자 개발된 NQ 유도체 물질은 0.2 µM 농도에서 대상 종인 Stephanodiscus sp. 종에 대하여 >80%의 높은 살조효과를 나타냈다. NQ 유도체 물질은 실험실 내 뿐만 아니라, 제어 효과를 변화 시킬 수 있는 다양한 요인이 존재하는 현장에서도 높은 제어 효과를 낼 수 있는 물질로서 실제 현장에서 적용할 수 있는 물질로 개발이 완료되었다고 사료된다. 더구나, NQ 유도체 물질은 분말 또는 액상 형태의 물질로서 현장 적용 시 수계의 규모 및 수심 등의 환경적 특징에 따른 적용 어려움 등의 문제점을 극복한 물질로 사용이 가능할 것으로 판단된다. 따라서, 본 연구를 통해 개발된 NQ 유도체 물질은 다양한 조건의 현장에서 Stephanodiscus sp. 종에 대한 방제와 발생을 사전에 막을 수 있는 예방 기술로서 사용이 가능할 것이다.