1. 서 론
2. 연구 방법
2.1 시료채취 및 수질분석
2.2 방류수 유기물질의 특성 분석
2.3 비스페놀 A의 등온 흡착 실험
2.4 에스트로겐 활성도 측정
3. 결과 및 고찰
3.1 방류수 유기물질의 물리화학적 특성
3.2 방류수 유기물질의 BPA 흡착
3.3 방류수 유기물질의 BPA 에스트로겐 활성 저감
4. 결 론
1. 서 론
하폐수처리장으로부터 수계로 유입되는 방류수 유기물질 (effluent organic matter, EfOM)은 자연 유기물질 (natural organic matter, NOM), 단백질, 탄수화물 등의 다양한 성분으로 이루어져 있어 수계 유기물질의 주요 공급원이 되는 것으로 알려져 있다. 일반적으로, 유기물질은 0.45 µm을 기준으로 입자성 (particular organic matter, POM)과 용존성 유기물질 (dissolved organic matter, DOM)로 분류하는데, 용존성 방류수 유기물질 (dissolved effluent organic matter, dEfOM)은 EfOM의 90% 이상을 차지한다 (Thurman 1985). 특히 dEfOM은 중금속과 유기화합물의 거동 및 생물유효도에 큰 영향을 미칠 수 있으며 (Baken et al. 2011, Yoo et al. 2016), 수서 생물에 직접적인 악영향을 미칠 수도 있다 (Yoo et al. 2019).
최근 친수성이 높은 EfOM이 소수성의 NOM과는 다른 물리화학적 특성을 가지며, 이들 특성의 차이가 Cu, Ag, Zn 등 미량 중금속과의 결합 및 독성에 큰 영향을 미치는 것으로 보고되었다 (Louis et al. 2014; Yoo et al. 2016). Liu et al. (2005)은 용존성 NOM이 내분비계 장애물질 (endocrine disrupting chemicals, EDCs)의 흡착에 중요한 역할을 한다고 보고하였으며, Lee et al. (2012)은 dEfOM이 강과 호수의 NOM보다 17β- estradiol (E2)의 흡착능이 4배 이상 높게 나타남을 확인하였다. 이를 통해 EfOM이 수환경 내 미량오염물질의 거동에 중요한 역할을 하는 것을 알 수 있다.
한편, 비스페놀 A (bisphenol A, BPA)는 페녹시수지, 합성수지 등 플라스틱 제조의 원료로 쓰이며, 내분비계 교란을 일으키는 대표적인 EDCs이다 (Sun et al. 2010). BPA는 하폐수처리장 방류수 뿐만 아니라 수환경 내에서도 여전히 발견되고 있으며, 이들이 수생태계에 미치는 악영향은 매우 크다 (Vandenberg et al. 2010). 최근 수계 내 부유물질이나 DOM에 흡착된 EDCs가 다양한 수준의 내분비계 장애 영향을 유발한 연구 (Tanghe et al. 1999)와 EfOM에 의한 E2 흡착이 에스트로겐 활성을 저감 시킨 연구 (Lee et al. 2011) 등이 보고되었다. 또한, Chen et al. (2012)은 용존성 NOM의 농도에 따라 E2의 에스트로겐 활성이 크게 달라짐을 규명하였다. 이를 통해 DOM이 에스트로겐성 물질의 거동 및 활성 변화에 중요한 역할을 한다는 것을 알 수 있다. 따라서 본 논문에서는 dEfOM이 BPA의 흡착과 에스트로겐 활성에 미치는 영향을 연구하였다.
2. 연구 방법
2.1 시료채취 및 수질분석
본 연구에 사용된 방류수 (SE1과 SE2)는 서울시에 위치한 2곳의 공공하수처리시설에서 2015년 4월 30일 오후 2 - 5시에 채취하였다. SE1과 SE2 하수처리시설은 모두 활성슬러지법을 이용하여 생활하수를 처리하였으며, 처리 용량은 각각 1,630,000과 900,000 m3 d-1이다. 각 방류수 시료의 pH, 용존산소 (dissolved oxygen, DO), 전기전도도는 현장에서 수질 다항목 측정기 (YSI-556, Yellow Springs Ins. USA)를 이용하여 측정하였다. 그리고 용존유기탄소 (dissolved organic carbon, DOC) 농도는 채수한 방류수 시료를 0.45 µm GF/C (Whatman, UK) 필터로 여과한 후 총 유기탄소 분석기 (TOC analyzer, Shimadzu 5000A, Japan)를 사용하여 측정하였다.
2.2 방류수 유기물질의 특성 분석
용존성 방류수 유기물질은 방류수 시료를 0.45 µm GF/C (Whatman, UK) 필터로 여과하여 사용하였다. 그리고 EfOM과의 비교연구를 위하여, IHSS (International Humic Substance Society)에서 구입한 Suwannee river NOM (SR-NOM)을 표준 NOM으로 사용하였다. 희석용액은 이온화 세기의 영향을 배제하기 위하여 담수의 이온화 세기와 유사한 0.01 M KNO3을 사용하였다.
유기물질의 화학적 특성은 자외선 흡광도와 형광 분석을 이용하여 측정하였다. 먼저 Mecasys사의 UV-Vis Spectrophotometer (model Optizen POP, Korea)를 이용하여 UV 254 nm에서 흡광도를 측정하였다. 그리고 측정한 흡광도 값은 DOC 농도로 나눈 후 100을 곱하여 특이 자외선 흡수 (specific UV absorption, SUVA) 값을 구하였다. 형광 지표 (fluorescence index, FI) 분석은 분광 형광계 (Spectrofluorometer, Hitachi F-7000, Japan)를 이용하였다 (Yoo et al. 2014). 시료의 inner-filter correction 과정을 생략하기 위하여 각 분리한 시료를 UV 254 nm에서 측정한 흡광도가 0.05 이하가 되도록 희석하였다 (Baker 2001). 또한 2차 Rayleigh 산란을 제거하기 위하여 램프 앞에 290 nm cut-off 필터를 사용하였으며, 370 nm 여기파장과 450과 500 nm 방출파장을 측정하여 이들의 비 (F450/F500)를 계산하였다.
2.3 비스페놀 A의 등온 흡착 실험
본 연구에 사용된 BPA (≥99%)는 Sigma-Aldrich사 (USA)의 제품을 구입하였으며, 탈이온수 (Puris Esse-UP ultrapure water System, Mirae St Corp., Korea)를 이용하여 고농도의 표준용액을 제조한 후 실험 전 초기농도를 1.0 × 10-2 M로 희석하여 실험에 사용하였다. BPA 실험 농도는 기존의 연구결과와 수환경 중에 존재하는 일반적인 농도를 바탕으로 선정하였다. BPA 농도를 확인하기 위하여 가스크로마토그래피 (GC-MSD 7890, Agilent, USA)를 이용하여 분석하였다. 시료의 농축을 위하여 DSC-18 (Supelco, USA) 카트리지를 이용한 고상추출법을 사용하였으며, 시료 10 mL를 1 mL min-1의 유속으로 통과시킨 후 메탄올로 용출시켜 분석하였다. BPA의 GC분석 조건은 Kang et al. (2010)에 명시된 분석 조건을 이용하였다.
분리한 dEfOM (5 mg C L-1)을 삼각플라스크에 주입하고 BPA 표준 용액을 이용하여 10-4 - 10-10 M이 되게 제조하여 shaking incubator에서 150 rpm으로 24시간 교반 하였다. 모든 등온 흡착 실험은 세 번 반복 하였으며, 광분해에 의한 영향을 배제하기 위하여 갈색시험관을 호일로 감싸서 사용하였다. 흡착 반응이 종료된 시료는 4000 g에서 20분 간 고속 원심분리한 후 상등액을 분리하여, 최종 BPA 농도 측정에 사용하였다. 그리고 흡착 실험 결과는 다음과 같은 Langmuir 등온 흡착식 (1)와 Freundlich 등온 흡착식 (2)으로 분석하였다.
| $$q_e=\frac{K_LQ_{max}C_e}{1+K_LC_e}$$ | (1) |
| $$q_e=K_F\;C_e^{1/n}$$ | (2) |
여기서 KL (L mg-1)과 KF ([mg g-1][mg L-1]1/n)는 각각 Langmuir와 Freundlich 상수이고, Qmax는 평형조건에서의 최대 흡착량 (mg g-1)이다. Ce (mg L-1)는 평형상태에서 용액 중 BPA의 농도이고, qe (mg g-1)는 평형조건에서 유기물질에 흡착된 BPA의 양이며, n은 흡착 강도와 연관된 Freundlich 상수다. 그리고 모든 실험 데이터는 SigmaPlot 프로그램 (Version 12.0, Systat Software Inc., USA)을 이용하여 비선형 회귀 분석을 실시하였다.
2.4 에스트로겐 활성도 측정
에스트로겐 활성도를 측정하기 위하여 형질변환 효모를 이용한 yeast two-hybrid assay를 이용하였다 (Shiraishi et al. 2003). 본 연구에 사용된 효모는 쥐의 에스트로겐 수용체 (rER)가 도입된 형질변환 효모 (Saccharomyces cerevisiae Y190)로서, 발현 효소의 정량은 Pierce사 (Thermo, USA)의 yeast β-galactosidase kit를 이용하였다 (Yoo et al. 2016). 간단히 설명하면, 먼저 형질변환 효모를 MSD 배지에서 30°C에서 48시간 배양하였다. 여기에 시료를 혼합하여 30°C에서 4시간 동안 배양하고, 660 nm에서 흡광도 (OD660)를 측정하여 효모의 균체량을 확인하였다. 그 후 buffer가 포함된 yeast extraction reagent을 첨가하여 37°C에서 발색 시키고, 시료의 발색이 확인되면 정지 시약을 주입한 후 420 nm에서 발색량 (A420)을 측정하였다. 그리고 assay kit에 명시된 식 (3)을 이용하여 에스트로겐 활성도 (estrogenic activity, EA)를 산출하였다.
| $$\mathrm{EA}=\frac{1,000\times{\mathrm A}_{420}}{\mathrm t\times\mathrm V\times OD_{660}}$$ | (3) |
t = time of incubation (min)
v = volume of cells (ml) used in the assay
에스트로겐 활성도를 비교 평가하기 위하여 양성대조로서 17β-estradiol (E2)을 사용하였으며, 적정 농도인 10-5 - 10-13 M의 범위에서 측정하였다. E2의 최대 활성도를 100%로 식 (4)를 이용하여 상대 에스트로겐 활성도 (relative estrogenic activity, REA)를 산출하였다.
| $$\mathrm{REA}=\frac{{\mathrm{EA}}_{\mathrm{sample}}}{EA_{\mathrm{maximum},\;\mathrm E2}}\times100$$ | (4) |
EAsample = estrogenic activity of sample
EAmaximum, E2 = maximum estrogenic activity of 17β- estradiol (E2)
또한, 각 화학물질의 농도에 따른 에스트로겐 활성도를 나타내는 농도-반응 곡선은 SigmaPlot 프로그램 (Version 12.0, Systat Software Inc., USA)을 이용하여 나타내었다.
3. 결과 및 고찰
3.1 방류수 유기물질의 물리화학적 특성
각 하수처리장 방류수 (SE1과 SE2)의 DOC 농도는 각각 6.15와 7.26 mg L-1로 유사한 값을 보여주었는데 (Table 1), 이는 국내에서 보고된 공공하수처리시설 방류수 DOC 농도 4.1 - 7.4 mg L-1 범위에 포함된다 (Cho et al. 2014). 용존성 방류수 유기물질 (SE-dEfOM)은 3 이하의 낮은 SUVA 값을 나타내었으나, 용존성 자연유기물질 (SR-NOM)은 4.4로 상대적으로 높은 값을 보여주었다 (Table 2). 보통 SUVA 값의 증가는 유기물 구조 중 이중결합 탄소 구조 및 방향족 성분의 분포가 상대적으로 많음을 설명한다 (Chin et al. 1997). 그리고 SUVA 값이 4에 가까운 경우 상대적으로 소수성이 크고 리그닌이 많은 육상 기원성 유기물질로 설명할 수 있고, 3 이하는 친수성이 높은 미생물 기원성 유기물질로 구분할 수 있다 (Quaranta et al. 2012). 이를 통해 SE-dEfOM은 SR-NOM에 비해 친수성이 높은 미생물 기원성 유기물질이 주로 분포하는 것을 알 수 있으며, 이는 최근 논문들의 결과와도 일치한다 (Quaranta et al. 2012, Yoo et al. 2014). 한편, 표준물질로 사용된 SR-NOM은 방향성이 높은 육상기원성 유기물질로 잘 알려져 있어, 높은 SUVA 값을 보여준 것으로 판단된다 (Leenheer 1994).
형광지표 (FI) 분석 결과 (Table 2), SE-dEfOM은 대체로 2에 가까운 값을 나타내었고, SR-NOM은 1.3에 가까운 낮은 값을 나타내었다. FI는 유기물질의 발생 기원을 확인하는 방법으로서 값이 낮을수록 높은 방향성 (aromaticity)을 나타내는데, 이 값이 1.3에 가까울수록 육상 기원성 유기물질로 구분하고 2에 가까울수록 미생물 기원성 유기물질로 구분할 수 있다 (Hur and Schlautman 2003, Leenheer and Croue 2003). 따라서 SE-dEfOM의 낮은 FI 값은 하수처리공정의 생물학적 처리에서 생성되는 유기산, 아미노산 및 탄수화물 등의 방향성이 낮은 물질들 때문인 것으로 설명할 수 있다 (Quaranta et al. 2012). 또한, SR-NOM은 주로 소수성이 높은 육상 기원성 유기물질로 이루어져 낮은 FI 값이 나타난 것으로 판단되며, 이는 상기의 SUVA 분석 결과와도 일치한다.
Table 1. Chemical properties of sewage effluent samples used in this study
| Effluent | pH | DO (mg L-1) | Conductivity (mS cm-1) | DOC (mg L-1) |
| SE1 | 6.86 | 12.1 | 0.57 | 6.15 |
| SE2 | 7.15 | 11.5 | 0.59 | 7.26 |
Table 2. Specific UV absorbance (SUVA) and fluorescence index (FI) of sewage effluent organic matter (SE1- and SE2-dEfOM) and Suwannee River natural organic matter (SR-NOM)
| Samples | SUVA (L m-1 mg-1) | FI |
| SE1-dEfOM | 2.71 | 1.87 |
| SE2-dEfOM | 2.52 | 1.90 |
| SR-NOM | 4.43 | 1.38 |
3.2 방류수 유기물질의 BPA 흡착
SE-dEfOM과 SR-NOM에 의한 BPA의 흡착 거동을 해석하기 위하여, 평형상태에서 얻어진 흡착 실험의 결과들을 Langmuir와 Freundlich 등온 흡착 모델에 적용하였다. 그 결과, Langmuir와 Freundlich 모델의 결정계수는 둘 다 r2 = 0.99 - 1.00으로 매우 높게 나타났으며 (Table 3), 이는 두 모델 모두 SE-dEfOM과 SR-NOM에 대한 BPA의 등온 흡착 거동을 잘 설명하는 것을 의미한다. 일반적으로 Langmuir 모델은 균일한 흡착제 표면에 대한 단층 흡착 (monolayer adsorption)을, 그리고 Freundlich 모델은 불균일한 흡착제 표면에 대한 다층 흡착 (multilayer adsorption)을 가정하고 있다. 방류수 유기물질이 균일한 화합물이 아니라는 것을 고려할 때, BPA는 불균일한 에너지를 갖는 표면에 흡착되었을 것으로 판단된다 (Lee 2017).
Table 3. Langmuir and Freundlich parameters for bisphenol A (BPA) binding onto sewage effluent organic matter (SE1- and SE2-dEfOM) and Suwannee River natural organic matter (SR-NOM). The parameters were determined using Eqs. (1) and (2) in text (n = 3)
Langmuir 모델에서 Qmax 값은 이론적인 최대 흡착량을 나타내는 계수로서 값이 클수록 흡착능이 큰 것으로 평가된다. SE1-와 SE2-dEfOM의 Qmax 값 (각각 8.142와 20.71 L mg-1)은 SR-NOM (6.761 L mg-1) 보다 높은 값을 나타냈다. 또한 Freundlich 모델에서 1/n은 화학적 결합에 의한 흡착 친화도를 의미하는데, 이 값이 >1, 1, <1 일 때 각각 S형, C형 그리고 L형 등온 흡착 특성을 갖는다 (Na et al. 2011). 본 연구에서는 모든 유기물질의 1/n 값이 1 보다 작은 L형 흡착 특성을 보여주었는데, 이것은 흡착질이 흡착제의 표면에 단층으로 흡착하는 경우에 나타나는 것으로 알려져 있다. 이를 통해 SE-dEfOM과 SR-NOM에 대한 BPA의 흡착은 단분자층의 화학흡착으로 생각된다.
Zhu et al. (2012)의 연구에서 DOM은 BPA와 주로 수소 결합 (hydrogen bonding)을 이루며, 특히 dEfOM에 포함된 다수의 페놀 분자들 (phenol molecules)이 BPA의 히드록시기 (hydroxyl group)와의 결합에 영향을 줄 수 있다고 보고하였다. 이를 통해 dEfOM에 포함된 다양한 유기물 성분이 BPA와의 결합에 큰 영향을 주는 것으로 판단할 수 있다. 또한 수용액 내 염석 효과 (salting-out effect)가 BPA의 흡착에 영향을 미칠 수 있으나, Shareef et al. (2006)는 0 - 0.1 M KNO3의 이온 강도는 BPA의 용해도에 영향을 미치지 않는다고 보고한 바 있으며, 본 연구에서는 0.01 M KNO3을 사용하였다.
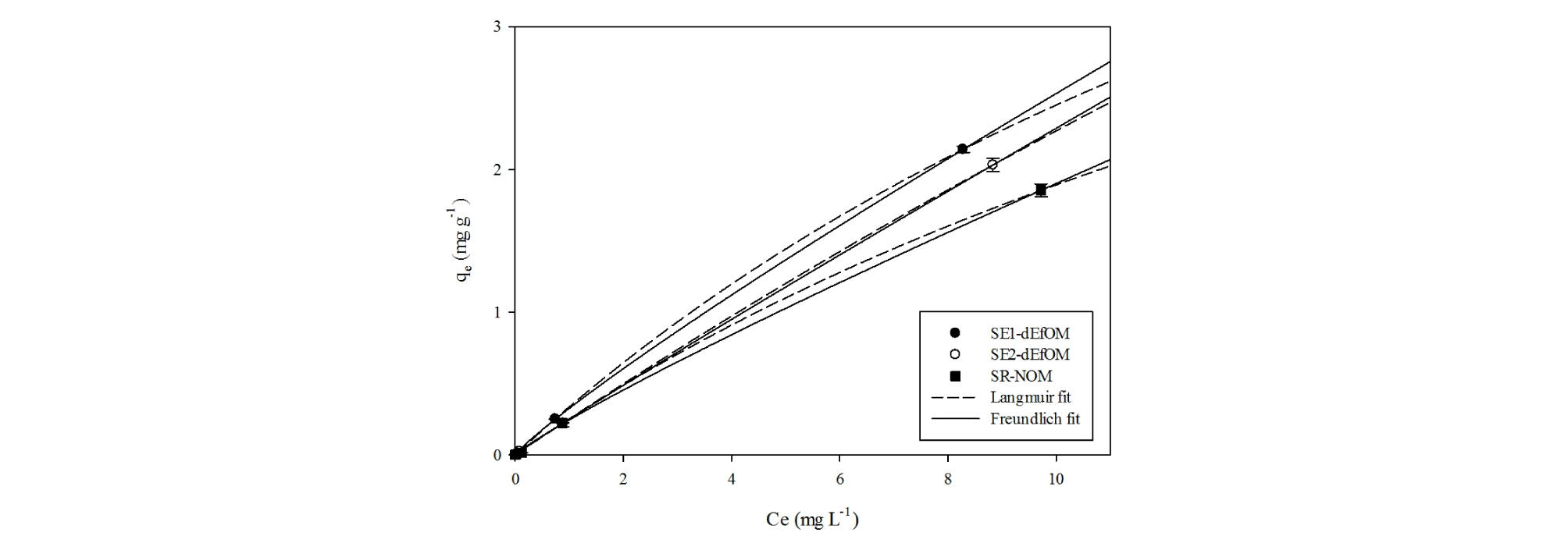
Fig. 1.
Absorption isotherms of bisphenol A onto sewage effluent organic matter (SE1- and SE2-dEfOM) and Suwannee River natural organic matter (SR-NOM). Background electrolyte was 0.01 M KNO3 and the concentration of dissolved organic matter was 5.00 mg C L-1. The experimental data were fitted using Eqs. (1) and (2) in text (n = 3).
3.3 방류수 유기물질의 BPA 에스트로겐 활성 저감
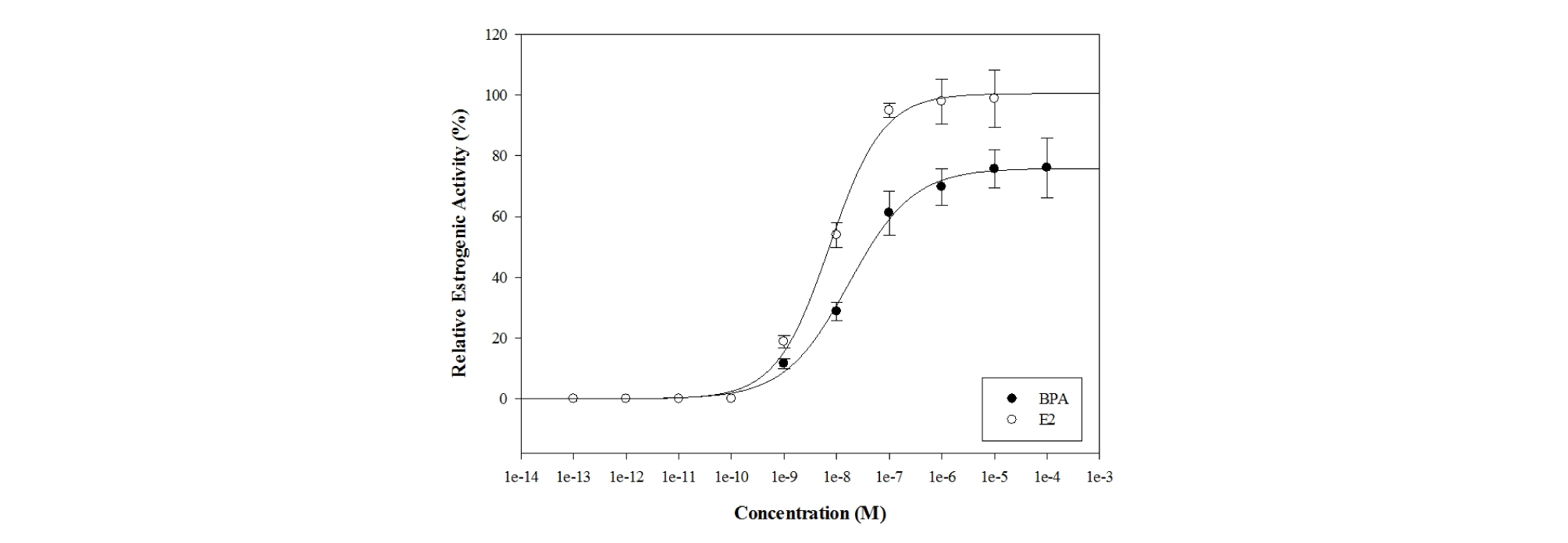
SE-dEfOM과 SR-NOM이 BPA의 에스트로겐 활성에 미치는 영향은 yeast two-hybrid assay를 이용하여 분석하였다. BPA와 E2의 농도에 따른 에스트로겐 활성도를 식 (5)의 회귀식으로 분석한 결과, 농도-반응 곡선이 높은 상관성 (각각 r2 = 0.9970과 0.9963)의 로지스틱 시그모이드 형태를 나타내었다 (Fig. 2).
| $$\mathrm Y=\frac a{1+({\displaystyle\frac x{x_0}})^b}$$ | (5) |
a = maximum relative estrogenic activity
b = minimum relative estrogenic activity
x0 = EC50 (50% effective concentration of estrogenic chemicals)
양성대조로 사용된 E2의 EC50 값을 각 화학물질의 EC50 값으로 나누어 상대강도를 산출한 결과 (Table 4), BPA의 에스트로겐 활성도는 E2보다 2.3배 정도 낮게 나타났다.
SE-dEfOM과 SR-NOM에 의한 BPA의 농도-반응 곡선은 Fig. 3에 나타내었으며, 상대 에스트로겐 활성도의 EC50값을 계산하여 Table 5에 나타내었다. 유기물질이 없는 조건에서 BPA의 상대 에스트로겐 활성도의 EC50값은 0.017 μM을 보여주었지만, 유기물질이 있는 조건 (SE-dEfOM과 SR-NOM)에서는 3.310 – 6.683 µM의 높은 EC50값이 나타났다. 이를 통해 BPA의 에스트로겐 활성은 유기물질이 있을 때 더 크게 감소함을 알 수 있으며, 유기물질에 의한 BPA의 흡착 및 독성 감소는 다른 연구를 통해서도 잘 알려져 있다 (Gattullo et al. 2012). 또한 SE-dEfOM의 EC50 값이 SR-NOM보다 더 크다는 것은 BPA의 상대 에스트로겐 활성도가 더 많이 감소하였다는 것을 나타낸다. 이는 상기의 등온 흡착 결과에서 SE-dEfOM이 SR-NOM에 비해 높은 BPA 흡착능을 나타낸 것으로 설명할 수 있다. 유기물질의 특성 분석에서 SE-dEfOM은 SR-NOM 보다 친수성이 높은 미생물 기원성 유기물질이 많이 분포하는 것을 확인하였는데, dEfOM에 포함된 다당류, 폴리페놀, 아미노산 등 다량의 단백질성 유기물질이 소수성의 유기화합물질과 강하게 흡착하여 생물 독성을 감소시킬 수 있다 (Chefetz et al. 2006, Pan et al. 2008).
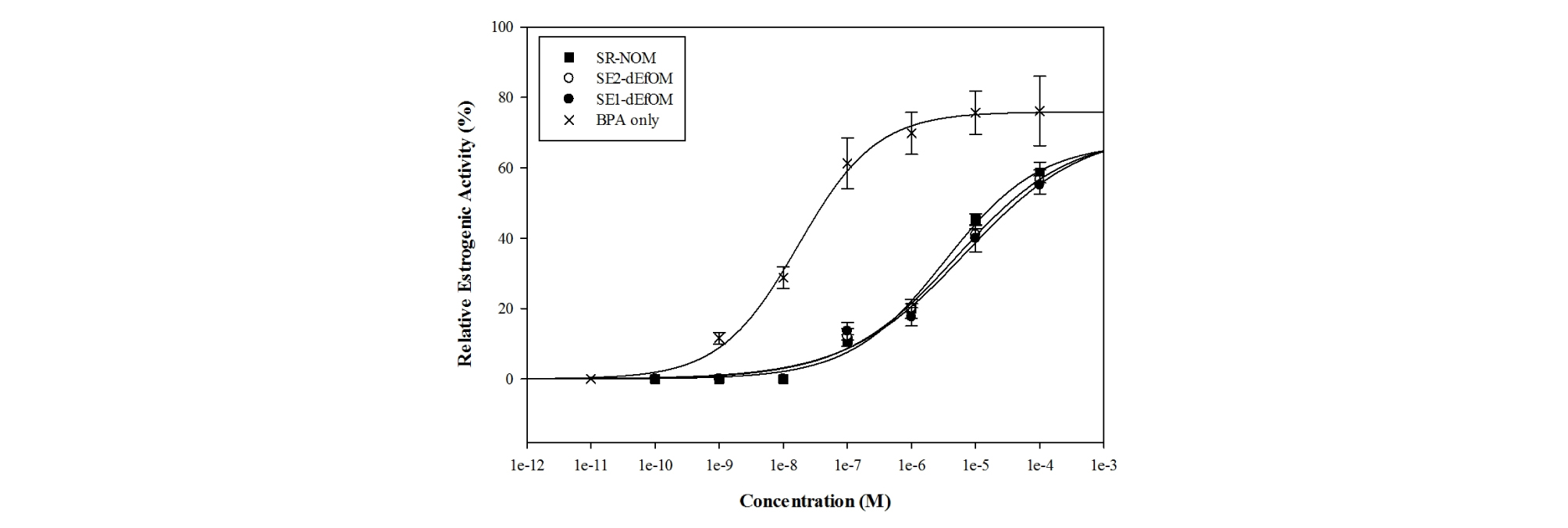
Fig. 3.
Concentration-response curves of bisphenol A (BPA) in the presence of sewage effluent organic matter (SE1- and SE2-dEfOM) and Suwannee River natural organic matter (SR-NOM). The concentration of dissolved organic matter was 5.00 mg C L-1.). The experimental data were fitted using Eq. (5) in text (n = 3).
Table 4. Regression parameters for concentration-response curve of bisphenol A (BPA) and 17β-estradiol (E2). The parameters were determined using Eq. (5) in text (n = 3)
| Parameters | BPA | E2 |
| a | 75.902 | 100.50 |
| b | -0.7113 | -0.8562 |
| x0 (M) | 1.7047 × 10-8 | 7.3240 × 10-9 |
| r2 | 0.9970 | 0.9963 |
| Relative potency | 0.4297 | 1.0000 |
Table 5. Effect of sewage effluent organic matter (SE1- and SE2-dEfOM) and Suwannee River natural organic matter (SR-NOM) on estrogenic activity of bisphenol A (BPA). Results are presented as the median effective concentration (EC50) The parameter was determined using Eq. (5) in text (n = 3)
| Samples | EC50 (μM) |
| BPA alone (positive control) | 0.017 ± 0.002 |
| SE1-dEfOM | 6.683 ± 8.126 |
| SE2-dEfOM | 5.038 ± 3.693 |
| SR-NOM | 3.310 ± 1.553 |